گروهی از پژوهشگران آمریکایی در مطالعه اخیرشان، از ویروس های باکتری خوار برای درمان عفونت های پیچیده ریه استفاده کردند.
به گزارش ایسنا به نقل از اس تی دی، بیست عفونت پیچیده و مقاوم به آنتی بیوتیک ریه توسط پژوهشگران دانشکده پزشکی دانشگاه کالیفرنیا سن دیگو و دانشگاه پیتسبرگ آمریکا با استفاده از ویروس های باکتری خوار درمان شدند. هیچ عارضه جانبی منفی پس از استفاده از این روش وجود نداشت و بیش از نیمی از بیماران تحت درمان، نتایج بالینی مطلوبی داشتند.
احتمال آنکه بیماران مبتلا به فیبروز سیستیک (Cystic Fibrosis) یا سایر اختلال های مزمن که طی آن نایژه های ریه (شبکه ای از لوله هایی که اکسیژن و سایر گازها را در سراسر اندام ها حمل می کنند) آسیب دیده یا از بین میرود، به عفونت های غیر مایکوباکتریوم توبرکلوزیس (NTM) مبتلا شوند، بالاتر است. عفونت های غیر مایکوباکتریوم توبرکلوزیس (NTM) بطور فزاینده ای در میان بیماران مبتلا به فیبروز سیستیک یا سایر بیماری های مزمن، شایع است.
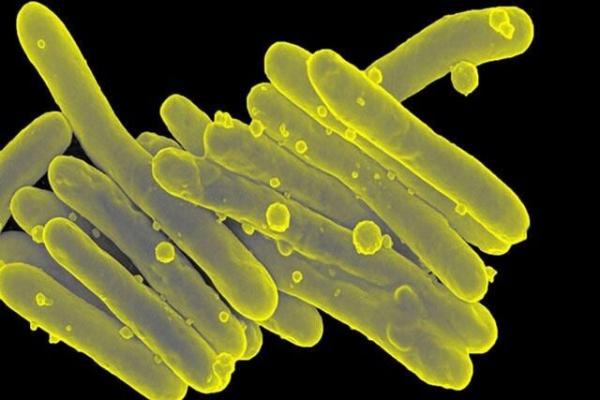
به دلیل مقاومت باکتریایی به آنتی بیوتیک ها، درمان عفونت های غیر مایکوباکتریوم توبرکلوزیس به ویژه عفونت هایی که توسط "Mycobacterium abscessus" ایجاد می شوند ، چالش برانگیز است. بر اساس گزارش مرکز کنترل و پيشگيري از بیماری های آمریکا (CDC)، سالانه ۳۵ هزار نفر در ایالات متحده در اثر ابتلا به تقریبا سه میلیون عفونت که به همه آنتی بیوتیک ها مقاوم هستند، جان خود را از دست می دهند.
ویروس هایی که بعنوان باکتریوفاژ (bacteriophages) شناخته می شوند برای مورد هدف قرار دادن و از بین بردن گونه های باکتریایی خاص توسعه یافته اند. هر جا که باکتری ها (Bacterium) زندگی می کنند، فاژها ممکن است در تعداد بیشتری از سایر اشکال زنده یافت شوند. آنها برای اولین بار در اوایل قرن بیستم شناسایی شدند و از آن زمان با رشد و گسترش باکتری های مقاوم به آنتی بیوتیک، تحقیقات بیشتر و بیشتری بر روی آن ها برای تعیین پتانسیل دارویی آنها انجام شده است.
در سال ۲۰۱۶، دانشمندان و پزشکان دانشکده پزشکی دانشگاه کالیفرنیا سن دیگو از یک فاژ درمانی وریدی آزمایشی برای درمان و معالجه همکارشان دکتر "تام پترسون" که بر اثر عفونت باکتریایی مقاوم به چند دارو در حال فوت بود استفاده کردند. این درمان موفقیت آمیز بود. پترسون، اولین مورد ثبت شده در ایالات متحده بود که از فاژهای داخل وریدی برای ریشه کن کردن عفونت باکتریایی سیستمیک در بدن وی استفاده شد. معالجه چند بیمار دیگر با این روش به ایجاد مرکز کاربردی و درمانی نوآورانه فاژ (IPATH) در دانشگاه کالیفرنیا سن دیگو منجر شد.
دکتر "کانستنس بنسون" (Constance Benson) استاد دانشکده پزشکی دانشگاه کالیفرنیا سن دیگو گفت: ما فکر می کنیم این یک موضوع و مطالعه انقلابی است که از نتایج آزمایش بیمار اصلی ما یعنی دکتر تام پترسون به دست آمد است.
در حال حاضر، کاربرد این روش محدود است و علت آن نیز تا حدی به این خاطر است که هرگونه فاژ تنها یک گونه باکتری را جستجو کرده و از بین می برد و تسلیحات فعلی فاژهای مفید شناخته شده از نظر درمانی، نسبتا کوچک است. در نتیجه، آزمایش فاژ درمانی در حال حاضر محدود به درمان های تجربی است که در آن همه درمان های جایگزین دیگر یا ناموفق هستند یا شکست خورده اند.
مطالعه جدید شامل گروهی متشکل از ۲۰ بیمار مبتلا به عفونت های مایکوباکتریایی پیچیده و مقاوم به آنتی بیوتیک بود. همه بیماران شرایط زمینه ای متفاوتی داشتند. اکثر آنها فیبروز سیستیک (CF) داشتند. فیبروز سیستیک یک بیماری ارثی و پیش رونده است که باعث آسیب شدید به ریه ها و سایر اندام ها می شود. در حال حاضر ، هیچ درمانی برای فیبروز سیستیک وجود ندارد. متوسط طول عمر (Longevity) افراد مبتلا به فیبروز سیستیک که تا بزرگسالی عمر می کنند تقریبا ۴۴ سال است.
بیماران شرکت کننده در این مطالعه بر اساس قانون "استفاده دلسوزانه" (compassionate use) سازمان غذا و داروی ایالات متحده واجد شرایط بودند. این قانون اجازه آزمایش داروها یا محصولات تحقیقاتی در شرایط تهدیدکننده حیات فرد و زمانی که هیچ درمان جایگزین قابل مقایسه یا رضایت بخشی وجود ندارد را می دهد.
بنسون و همکارانش در این مطالعه ۲۰۰ بیمار مبتلا به بیماری علامت دار ریه (Lung) را غربالگری کردند تا سویه های باکتریایی را که احتمالا به فاژها حساس هستند شناسایی کنند. محققان در نهایت ۵۵ سویه را شناسایی کردند سپس فاژها به ۲۰ شرکت کننده این مطالعه به صورت داخل وریدی یا توسط آئروسل سازی از طریق نبولایزر یا با استفاده از هر دو روش دو بار در روز طی یک دوره متوسط شش ماهه تجویز شدند، اگرچه برخی از بیماران درمان های کوتاه تر یا طولانی تری بر اساس پاسخ بالینی یا میکروبیولوژیک داشتند.
نبولایزر یا ریزپاش وسیله ای برای رساندن دارو به قسمت های مختلف دستگاه تنفس از طریق استنشاق می باشند، این درمان بخصوص در وضعیت هایی مانند برونشیت و آسم شدید بسیار مؤثر هستند و به دلیل سریع بودن تأثیر دارو و جلوگیری از تأثیر دارو بر بافت های دیگر بدن بسیار مورد توجه می باشد و با توجه به نوع داروی مصرفی باعث بهبود تهویه، افزایش عملکرد ماهیچه های تنفسی، بهبود استقامت فعالیت های عمومی، جلوگیری از تجمع ترشحات ریوی، بهبود سرفه، پيشگيري از آتلکتازی، کاهش چسبندگی، کمک به بازگشت خون، کاهش درد و کاهش اسپاسم می شود.
پس از آن بیماران از نظر عوارض جانبی، علائم بهبود یا کاهش حضور باکتری، ظهور مقاومت فاژی و یا خنثی سازی فاژها توسط سیستم ایمنی تحت نظر قرار گرفتند. نویسندگان بدون توجه به نوع عفونت باکتریایی یا انواع فاژهای مورد استفاده یا روش های درمانی استفاده شده، هیچ واکنش نامطلوبی به فاژ درمانی را در هیچ یک از بیماران گزارش نکردند. ۱۱ بیمار از ۲۰ بیمار تا حدودی بهبود علائم یا کاهش حضور باکتری را نشان دادند. پنج بیمار پیامدهای غیرقطعی داشتند و چهار بیمار هیچ پاسخی به درمان نشان ندادند.
بنسون گفت: باتوجه به پیچیدگی شرایط بیماران و شرایط فردی آن ها، نمی توان نتیجه گسترده ای گرفت ولی میتوان گفت درمان فاژی عفونت های مایکوباکتریایی امیدوارکننده است و باید بیشتر مورد بررسی قرار گیرد.
یافته های این مطالعه در مجله "Clinical Infectious Diseases" منتشر شده است.
- 13
- 3