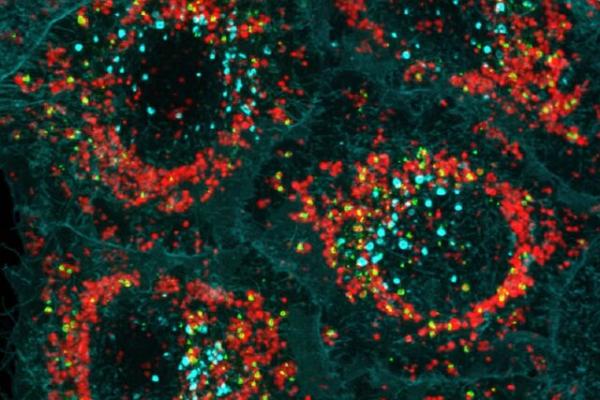
محققان ساز و کاری را کشف کرده اند که توسط آن پروتئینی موسوم به اپتینورین (optineurin) اصطلاحا «کیسه های زباله ای» را در اطراف میتوکندری های آسیب دیده ایجاد و آن ها را مستعد حذف می کند.
به گزارش ایسنا به نقل از نیو اطلس، به لطف تحقیقات جدید پژوهشگران استرالیایی که کشف کرده اند چگونه پروتئینی به نام اپتینورین به روشی متمایز برای پاک کردن میتوکندری های آسیب دیده از مغز کار می کند، ممکن است یک قدم به توسعه درمانی برای بیماری پارکینسون نزدیک تر شده باشیم.
بیماری پارکینسون یک اختلال پیش رونده، مخرب و درازمدت دستگاه عصبی مرکزی است که عمدتاً سیستم حرکتی بدن را مختل می کند. نشانه های این بیماری معمولاً آرام و به تدریج ظاهر میشوند و با پیشرفت بیماری، علائم غیرحرکتی نیز بروز می کنند. آشکارترین نشانه های زودرس این بیماری عبارتند از لرزش، خشکی در حرکت بدن، آرام شدن حرکات و دشواری در راه رفتن. نشانه های شناختی و رفتاری این بیماری نیز در اغلب افراد معمولاً به شکل افسردگی، اضطراب و فقدان علاقه و هیجان بروز می کند.
در مراحل پیشرفته بیماری پارکینسون (Parkinson's Disease)، بعضاً زوال عقل نیز شایع است. فرد مبتلا به پارکینسون امکان دارد مشکلاتی در خوابیدن و سیستم حواس خود نیز تجربه کند.
نشانه های حرکتی این بیماری به علت از بین رفتن سلول ها در توده سیاه مغز و در نتیجه کاهش دوپامین که یک انتقال دهنده عصبی است، رخ می دهد. دوپامین برای حفظ الگوهای حرکتی طبیعی بدن اهمیت زیادی دارد و دقیقاً به همین دلیل است که بسیاری از درمان های پارکینسون با هدف افزایش سطح دوپامین در مغز انجام می شوند.
در بیماری پارکینسون ، از بین رفتن نورون ها (یاخته های عصبی) در سایر بخش های مغز هم رخ می دهد و زمینه ساز برخی علائم غیرحرکتی این بیماری می شود. علاوه بر کاهش دوپامین و سلول هایی که دوپامین می سازند، پروتئینی به نام آلفا- ساینوکلین هم در بیماری پارکینسون نقش دارد. آلفا- سینوکلئین در حالت عادی به برقراری ارتباط نورون ها با یکدیگر کمک می کند، اما در بیماری پارکینسون ، این پروتئین در توده های میکروسکوپی به نام جسم لویی، جمع می شود. پژوهشگران بر این باورند که آلفا- سینوکلئین در پیشرفت پارکینسون نقش دارد و شاید بتوان درمان های جدیدی ایجاد کرد که جلوی جمع شدن این پروتئین را بگیرد.
اگرچه علت بروز بیماری پارکینسون کاملا مشخص نیست، اما می دانیم که هر دو فاکتور ژنتیکی و محیطی در بروز آن نقش دارند. از این میان می توان به فاکتورهایی مانند افزایش سن، پیشینه خانوادگی ابتلا به بیماری پارکینسون ، جهش های ژنتیکی، جنسیت، قرار گرفتن در معرض سموم دفع آفات، مصرف برخی داروها و پیشینه آسیب و جراحت مغز بعنوان عوامل بروز این بیماری اشاره کرد. مصرف کنندگان تنباکو و قهوه و چای، ریسک کمتری برای ابتلا به پارکینسون دارند.
تشخیص موارد معمول پارکینسون عمدتا بر اساس نشانه های این بیماری به خصوص نشانه های حرکتی انجام می شود. از آزمایش هایی مانند تصویربرداری عصبی می توان برای تشخیص قطعی و کنار گذاشتن سایر بیماری ها استفاده کرد. پارکینسون معمولاً در افراد بالای ۶۰ سال بروز می کند. مردان بیشتر از زنان به این بیماری مبتلا میشوند و نسبت ابتلای مردان به زنان ۳ به ۲ است. پارکینسون ممکن است در افراد زیر ۵۰ سال نیز ایجاد شود که در این صورت پارکینسون زودرس خوانده می شود. طبق آمار سال ۲۰۱۵ حدود ۶/۲ میلیون فرد در جهان مبتلا به پارکینسون هستند و این بیماری سالانه به بیش از ۱۱۷ هزار مرگ منجر می شود. امید به زندگی متوسط پس از تشخیص این بیماری، ۷ تا ۱۵ سال است.
تا کنون راهی برای علاج و رفع پارکینسون پیدا نشده اما روش هایی برای درمان و کاهش عوارض این بیماری وجود دارد. درمان اولیه معمولاً با تجویز دارو شروع می شود. با پیشرفت بیماری، اثر این داروها کمتر می شود و عوارض جانبی مانند دیسکینزی (حرکات غیرارادی عضلات) بروز می کند. در این مرحله، ممکن است داروها به صورت ترکیبی استفاده و دوز آن ها افزایش داده شود.
مشخص شده است که رژیم غذایی (diet) و برخی اشکال کاردرمانی در بهبود این علائم تا حدی مؤثر است. در مواردی که بیمار دچار علائم شدید حرکتی است و به دارو پاسخ نمی دهد، گاهی از جراحی برای قراردادن ریز الکترونیک و تحریک عمقی مغز استفاده می شود.
میتوکندری ها نیروگاه سلول های ما هستند. آنها اکسیژن را با مولکول های سوختی- قندها و چربی ها- از غذا ترکیب می کنند و آنها را برای تولید انرژی تجزیه می کنند. وقتی میتوکندری معیوب باشد، سلول ها انرژی کافی ندارند و مولکول های اکسیژن و سوخت استفاده نشده در سلول ها تجمع می کنند و باعث آسیب می شوند. میتوکندری های معیوب با بیماری های مختلفی از جمله بیماری پارکینسون مرتبط هستند.
وقتی میتوکندری ها تجزیه می شوند ، معمولاً توسط سیستم دفع زباله بدن در فرآیندی به نام میتوفاژی حذف و بازیافت می شوند. پژوهشگران موسسه والتر و الیزا هال (WEHI) مکانیسم های مولکولی زیربنای حذف میتوکندری های آسیب دیده ، به ویژه در شرایط بیماری پارکینسون را بررسی کردند و به کشف مهمی در این فرآیند رسیدند.
روشی که بدن میتوکندری های آسیب دیده را به واسطه آن حذف می کند، یک فرآیند آبشاری است. پروتئین PINK1 سلامت میتوکندری را کنترل می کند و هنگامی که مشکلی تشخیص داده می شود، پروتئین دیگری به نام پارکین را فعال می کند تا میتوکندری آسیب دیده را برای حذف علامت گذاری کند. سپس این دو پروتئین از پروتئین سوم که همان اپتینورین (OPTN) است، کمک می گیرند تا یک کیسه زباله سلولی در اطراف میتوکندری های ناکارآمد ایجاد کنند.
البته همه ی اینها را پژوهشگران قبلا می دانستند. با این حال، آنچه آنها در مطالعه جدید خود کشف کردند این است که اپتینورین، میتوکندری های آسیب دیده را با اتصال به آنزیمی به نام TBK1 شناسایی و حذف می کند.
در حالی که پژوهشگران از وجود اپتینورین و نقش آن در این فرآیند آگاه بودند، ولی نحوه عملکرد آن تاکنون ناشناخته بود.
مایکل لازارو، نویسنده مسوول این پژوهش می گوید: در حالی که پروتئین های زیادی وجود دارند که مواد سلولی آسیب دیده را به ماشین های دفع زباله مرتبط می کنند، ما متوجه شدیم که اپتینورین این کار را به روشی بسیار غیرمتعارف انجام می دهد که شبیه چیزهایی نیست که در پروتئین های مشابه دیده ایم.
او ادامه داد: این یافته بسیار مهم است، زیرا مغز انسان برای تخریب میتوکندری خود از طریق سیستم دفع زباله که توسط PINK1 و پارکین هدایت می شود، به اپتینورین متکی است.
در بیماری پارکینسون، جهش در PINK1 و پارکین می تواند منجر به تجمع میتوکندری های آسیب دیده در مغز شود که منجر به لرزش و سفتی می شود که نشانه های بیماری تخریب عصبی است. پژوهشگران می گویند کشف تعامل OPTN با TBK1 می تواند به درمان های جدیدی ختم شود.
تان انگوین، نویسنده ارشد این مطالعه می گوید:سایر پروتئین ها برای کمک به تحریک این فرآیند تخریب، به TBK1 نیاز ندارند و اپتینورین را در مورد نحوه حذف میتوکندری ها در بدن ما به یک ماده نامربوط تبدیل می کند. این به ما این امکان را می دهد تا به ویژگی های این مسیر شامل TBK1 به عنوان یک هدف دارویی بالقوه نگاه کنیم که گام مهمی در جستجوی ما برای درمان های جدید بیماری پارکینسون است.
پژوهشگران می گویند، این کشف، راه را برای توسعه درمان هایی باز می کند که از مکانیسم عمل OPTN استفاده می کنند.
انگوین می گوید:هدف نهایی، یافتن راهی برای افزایش سطح میتوفاژی PINK1/Parkin در بدن- به ویژه مغز- خواهد بود تا میتوکندری های آسیب دیده را بتوان بطور مؤثرتری از بین برد.
او افزود: ما همچنین امیدواریم مولکولی طراحی کنیم که بتواند کاری که اپتینورین انجام می دهد را تقلید کند، بنابراین میتوکندری های آسیب دیده حتی بدون PINK1 یا پارکین نیز حذف می شوند. با توجه به اینکه اپتینورین در فعال کردن سیستم دفع زباله در مغز ما حیاتی است، می تواند از تجمع میتوکندری های آسیب دیده در این ناحیه که پیش ساز مهمی برای بیماری پارکینسون است، جلوگیری کند.
در حالی که تا به کار گرفتن بالینی یافته های این مطالعه سال ها فاصله داریم، تحقیقات بیشتری برای درک بهتر اینکه چرا اپتینورین چنین کاری را انجام می دهد، برنامه ریزی شده است.
انگوین در پایان گفت: گام بعدی ما همکاری با مرکز بیماری پارکینسون WEHI است تا یافته هایمان در سیستم های مدل عصبی را تأیید کنیم و بفهمیم چرا اپتینورین به این شکل رفتار می کند که بینش بیشتری در مورد اینکه چگونه می توانیم اپتینورین و TBK1 را هدف قرار دهیم، به دست بیاوریم و گزینه های درمانی برای افراد مبتلا به جهش پارکین یا PINK1 را در آینده افزایش دهیم.
بیماری پارکینسون نخستین بار توسط یک دانشمند بریتانیایی به نام جیمز پارکینسون در سال ۱۸۱۷ میلادی توصیف شد و بنابراین نام او را روی این بیماری گذاشتند. کارزارهای افزایش آگاهی درباره این بیماری عبارتند از روز جهانی پارکینسون (۱۱ آوریل، روز تولد جیمز پارکینسون) و استفاده از گل لاله سرخ بعنوان نماد و سمبل این بیماری.
این مطالعه در مجله Molecular Cell منتشر شده است.
- 9
- 1