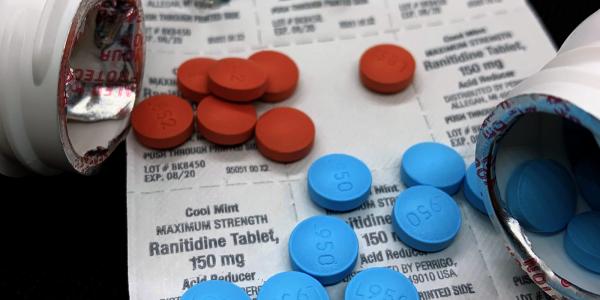
به گزارش باشگاه خبرنگاران، بر اساس اعلام اداره غذا و دارو( FDA)، از ابتدای ماه آوریل ( ۱۳ فروردین ماه) همه شکل های داروی رانیتیدین( زانتاک)، به علت احتمال آلودگی به ماده خطرناک و سرطان زای ان- نیتروزو- دی- متیل- آمین( NDMA)، باید از بازار جمع آوری شود. مطالعات نشان می دهد مقدار این ماده با گذشت زمان و نگهداری دارو در دماهای بالاتر، بیشتر می شود.
بر اساس اعلام سازمان غذا و دارو آمریکا در حال حاضر میزان آلودگی در بسياري از فرآورده های رانیتیدین امکان دارد پائین باشد، ولی با توجه به اینکه معلوم نیست این داروها تا چه زمان امکان دارد نگهداری شود، تصمیم گرفته شد همه انواع آن جمع آوری شود.
این بدان معنی است که محصولات رانیتیدین برای نسخه های جدید یا موجود یا استفاده بدون نسخه (OTC) در آمريکا دردسترس نخواهد بود.
FDA میزان N- nitrosodimethylamine) NDMA) را در بعضی از محصولات ranitidine با افزایش زمان و دما ایجاد می کند و این خطر را برای مصرفکنندگان افزایش می دهد، بدین ترتیب آژانس تقاضا کرده است که تمام محصولات رانیتیدین را از بازار آمریکا خارج کند.
مصرف کنندگان باید مصرف هر نوع فرآورده رانیتیدین OTC که در حال مصرف هستند با دستور پزشک خود جایگزین کنند.
بدین ترتیب هیچ کدام از انواع رانیتیدین موجود در بازار بی خطر نیست و به تمامی بیماران توصیه می شود از مصرف این دارو به هر شکل اکیدا پرهیز کنند.
تا به امروز، آزمایش FDA، NDMA را در محصولات مورد استفاده برای درمان مشابه مانند فاموتیدین( پپسید)، سایمتیدین( تاگامت)، استروسول( نکسیوم)، لانسوپرازول( Prevacid) یا امپرازول(Prilosec) پیدا نکرده است.
بیماران میتوانند با مشورت با پزشک خود، از داروهای مشابه مثل فاموتیدین، سایمتیدین، امپرازول، و ... استفاده کنند، چون بررسی های اداره غذا و دارو نشان می دهد که این داروها فاقد NDMA هستند.
- 13
- 6