تکنیک ویرایش ژنی کریسپر در سال های اخیر به یکی از امیدوارکننده ترین زمینه های زیست پزشکی تبدیل شده است، اما آیا در سال جاری شاهد اولین درمان های واقعی کریسپر خواهیم بود؟
سال ۲۰۱۲ بود که محققان دریافتند که سیستم ایمنی باکتریها میتواند برای اصلاح و تغییر دیانای سلولهای موجودات زنده، به کار گرفته شود. از همان زمان بود که کریسپر به عنوان تکنیکی انقلابی به جامعهی پزشکی و ژنتیک معرفی شد.
محققان آمریکایی در سال ۲۰۱۲ توانستند که برای درمان نوعی بیماری ژنتیکی مرتبط به قلب از این تکنیک نوظهور بهره ببرند. علاوه بر این، در سالهای پس آن نیز از تکنیک ویرایش ژنی کریسپر برای درمان بسیاری از بیماریها در محیط آزمایشگاهی استفاده شده است. حتی به گفته برخی، گریندرها هم از تکنیک کریسپر برای بهبود وضعیت جسمانی خود بهره میبرند!
گریندرها (Grinder)، تلاش میکنند با هک کردن بدن خود، مهارتهای فوقالعاده ای را در زندگی کسب کنند. در واقع به گفته گریندرها، بیوهک، خط مقدم نوع جدیدی از تکامل است. آنها با درهم آمیختن و گسترش حواس، امکان انجام کارهایی مانند شناسایی وای فای، شنیدن رنگها، تعیین مغناطیس شمال و دیدن در تاریکی را پیدا کردهاند.
اکنون در آغاز سال جدید میلادی هستیم، اگر سال ۲۰۱۷ را سالی بدانیم که تکنیک ویرایش ژنی کریسپر توانست قدرت واقعی خود را به همگان نشان دهد، آیا در سال ۲۰۱۸ واقعا شاهد درمان بیماریها با این تکنیک ژنتیکی انقلابی خواهیم بود؟
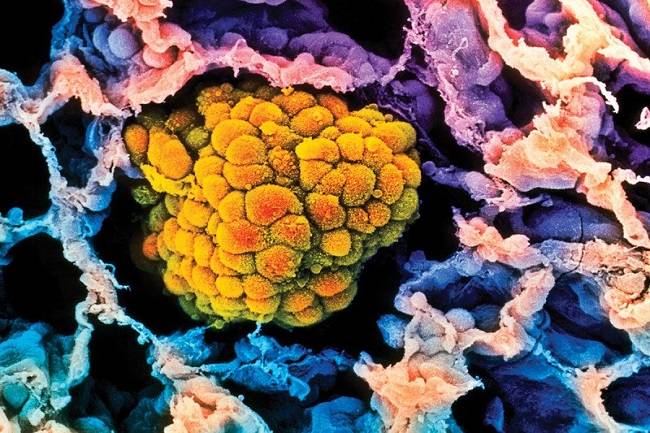
دانشمندان هنوز درگیر مناقشات اخلاقی این تکنولوژی هستند، این تکنولوژی با برش توالی ژنی قادر به کارهای عجیبی ازجمله، اصلاح ژنی حشرات ریزی که تارعنکبوت میبافند. از طرف دیگر، کودکانی که امروزه متولد شوند شاید دیگر هرگز مبتلابه بیماری والدین خود نشوند و حتی امکان اینکه بهطورکلی این سرطانهای ارثی از بین برود هم وجود دارد
کریسپر به توالیهای غیرمعمول دیانای اشاره دارد که به ارگانیسمها برای شناسایی تهدیدها -خصوصا ویروسها- کمک میکند. نام این روش مخفف تناوبهایِ کوتاهِ پالیندرومِ فاصلهدارِ منظمِ خوشهای است. در توالی دیانای، خوشهها در فواصل مشخصی از هم فاصله میگیرند و پالیندرومها در تکرارهای کوتاه با تغییرات اندکی بارها و بارها تکرار میشوند.
دانشمندان برای اولین بار در دهه ۱۹۸۰ زمانی که ژنوم آرکیها و باکتریها را مطالعه میکردند، متوجه این موضوع شدند. حتی در چنین ژنوم نسبتا سادهای، زیستشناسان متوجه شدند که این توالیهای عجیب به روشی بسیار خاص و بافاصله تکرار میشوند.
زیستشناسان مولکولی مطمئن بودند که آنها هدف منحصربهفردی دارند و نظریه متداول بهزودی تبدیل به دفاع ویروسی شد که در نهایت در سال ۲۰۰۷ تحت هدایت فیلیپ هورواث به اثبات رسید. با این وجود محققان از اوایل دههی ۲۰۱۰ و بهخصوص در مورد پتانسیل فوقالعاده بالای تکنیک کریسپر شور و اشتیاق خاصی از خود نشان دادهاند.
کریسپر را میتوان با ارسال کد مورس در تلگراف مقایسه کرد. هر دنباله حاوی پیامی در مورد حمله متفاوتی است و هر فضا توقفی است که پیام را به پایان میرساند. هنگامیکه یک ارگانیسم با یک ویروس جدید و خطرناک مواجه میشود، بدن نمیداند چگونه باید از خود محافظت کند و یا ویروس را از بین ببرد، این چیزی است که مانند بسیاری از پاسخهای سیستم ایمنی باید یاد بگیرد.
اما چنین چیزی میتواند دشوار باشد، چراکه ویروسها مستقیما به دیانای حمله میکنند، اما این همچنین باعث میشود ویروس از جهاتی آسیبپذیر باشد. کریسپر توالی رشتههای مهم دیانای ویروس را میقاپد و در پیامهای کد مورس نگه میدارد و هنگامیکه ویروس مشابهی دوباره حمله میکند، کریسپر آن پیام کد مورس را به میدان جنگ میفرستد.
به گفته محققان، قرار است که در سال ۲۰۱۸، اولین آزمایشهای کلینیکی کریسپر روی انسانها انجام شود. در همین راستا، شرکت کریسپر تراپیوتیکز، اولین برنامههای خود را برای انجام آزمایشهای کلنیکی به مراجع قانونی اروپا ارسال کرده است. در این آزمایشها که قرار است به زودی آغاز شود، از تکنیک ویرایش ژنی کریسپر به همراه اصلاح سلولهای بنیادی برای درمان بیماری بتا تالاسمی استفاده خواهد شد.

محققان قادر به جهش هدفمند هر دو موشی که آزمایش میکردند، شدند. اما آنها همچنین تعداد قابلتوجهی تغییرات اضافی دی ان ای- ۱۶۰۰ جهش ژنتیکی ناخواسته در نوکلئوتید هر موش – در نواحی از ژنوم شدند که قصد تغییر آن را نداشتند
سامارت کولکارنی، موسس و مدیرعامل کریسپر تراپیوتیکز، میگوید که شرکتش میخواهد، برنامه پیشنهادی مشابهی برای آزمایشهای کلینکی دیگری مرتبط به بیماران کم خونی داسی شکل را تا پایان نیمه اول سال جاری طرحریزی کند.
به گفته سامارت کولکارنی:
اولین انسان با تکنیک ویرایش ژنی کریسپر، در سال ۲۰۱۸ و در آزمایشگاه درمان میشود. ما میخواهیم نخستین محققانی باشیم که دست به این آزمایشها میزنیم.
بیماریهایی که از آنها نام برده شد، اختلالهای ژنتیکی مربوط به جهش ناخواسته ژنهایی هستند که تولید هموگلوبین میکنند. هموگلوبین پروتئین حیاتی است که با استفاده از گلبول های قرمز خون، اکسیژن و دیاکسیدکربن را به همه اندامهای حیاتی بدن منتقل میکند.
به این ترتیب، در صورتی که این پروتئین، دچار مشکل شود یا تضعیف شود، فرد به کم خونی شدید، ضعف عضلانی، رشد دیر رس و فشار خون مبتلا میشود. با این حال، محققان میگویند که با استفاده از تکنیک ویرایش ژنی کریسپر، میتوانند با اصلاح دیانای جان بسیاری از بیماران مبتلا به بیماریهای لاعلاج را نجات دهند و روزنهای امیدبخش را به سوی این دست افراد بگشایند.
در این مورد، افراد مبتلا به دو بیماری کمخونی داسی شکل و تالاسمی بتا، از آنجایی که در هر دوی این بیماری نوعی جهش ژنی در دیانای فرد به وجود میآید، ممکن است که از بهترین گزینهها برای درمان با تکنیک ویرایش ژنی کریسپر باشند.
محققان دانشگاه استنفورد در نظر دارند که از تکنیک ویرایش ژنی کریسپر برای درمان بیماریهای مرتبط به سلولهای بدخیم بهره ببرند. آنها تصمیم دارند که اولین آزمایشهای کلنیکی خود را تا پایان سال جدید انجام دهند.
متیو پوروتوس، سرپرست تیم تحقیقاتی استنفورد، میگوید که او و همکارانش برنامهی پیشنهادی خود برای انجام آزمایشهای کلنیکی را تا قبل از سال ۲۰۱۹ به سازمان غذا و داروی آمریکا (FDA) ارسال کرده و آزمایشهای خود را در سال آینده انجام میدهند.
تصویری که جورج چرچ را در کنار مخلق نیمه ماموت-فیل او نشان می دهد. چرچ در طول کنفرانس بوستون که یکی از موضوعات کلیدی مورد بحث آن ویرایش ژنی و پیامدهای اخلاقی آن بود، گفت، پروژه ماموت دو هدف را دنبال میکند، تضمین یک آینده جایگزین برای فیلهای آسیایی در معرض خطر و کمک به مقابله با گرمایش جهانی. ماموت پشمالو میتواند از ذوب پرمافراست تندرا جلوگیری کند و از انتشار میزان زیادی از گازهای گلخانهای بکاهد
متیو پوروتوس میگوید:
ما میخواهیم، در سال ۲۰۱۸، تا جای ممکن، اطلاعات ضروری را جمعآوری کنیم تا بتوانیم در سال ۲۰۱۹، آزمایشهای کلنیکی خود را آغاز کنیم.
اما، دانشمندان چینی پیش از این اقدام به انجام آزمایشهای کلینیکی روی انسان کردهاند. در بهار ۲۰۱۵ گروهی از دانشمندان چینی دیانای ۵۴ جنین را با استفاده از تکنیک ویرایش ژنی کریسپر اصلاح کردند. ۲۸ عدد از این جنینها با موفقیت اصلاح شدند، ولی ۲۶ جنین یعنی تقریبا نیمی از آنها، با شکست مواجه شد و به این ترتیب، آزمایش دانشمندان چینی بحثهای زیادی را در محافل علمی برانگیخت. آنها در سالهای بعد هم آزمایشهای مشابهی را تکرار کردند، چیزی که در نهایت نگرانیهای زیادی را در بین جوامع علمی مختلف جهان ایجاد کرد.
به گفته پوروتوس، انتظار میرود که تا پایان سال ۲۰۱۸، تحقیقات و مطالعات بیشتری برای کشف کاربردهای درمانی و پتانسیل تکنیک کریسپر انجام گیرد. سال گذشته، محققان توانستند که تحقیقات زیادی را برای شناخت بهتر بیماری مرگباری هم مانند هانتینگتون، بیماری لو گهرگیگ یا اسکلروز جانبی آمیوتروفیک و نوعی ناشنوایی در موشها انجام دهند.
پوروتوس میگوید که در سال جاری، آزمایشهای کلینیکی میتوانند، حتی پتانسیلهای بیشتری از تکنیک ویرایش ژنی کریسپر را به ما نشان دهند.
پرفسور جورج چرچ، یکی از مشهورترین افرادی است که از تکنیک کریسپر در تحقیقات خود بهره میگیرد. او اعلام کرده است که تکنیک کریسپر باید در سال ۲۰۱۸ دقیقتر از قبل شود. پرفسور چرچ همان مهندس ژنتیک مشهور دانشگاه هاروارد است که گفته بود، میتواند در عرض دو سال آینده جنین ترکیبی از ماموت پشمالو و فیل بسازد.
چرچ اعلام کرده است که در این پروژه ژنهای ماموت با استفاده از تکنیک ویرایش ژنی کریسپر به دیانای فیل متصل میشوند. او همچنین انتظار دارد که برخی بیماریهای مشترک بین انسان و حیوان هم مانند لایم و مالاریا و اصلاح ژنتیکی ارگاتهای قابل پیوند در خوکها نیز درمان شود.
هیجانانگیزترین آزمایش تکنیک ویرایش ژنی کریسپر در حال حاضر در چین در حال انجام است، جایی که دانشمندان در تلاشاند تا با استفاده از تکنیکهای کریسپر، دی ان ای آسیب دیده را از سلولهای زنده بیماران مبتلابه سرطان ریه حذف کنند

کوین اسولت، زیستشناسی مصنوعی از موسسه MIT میگوید، در سال ۲۰۱۸ قطعا شاهد پیشرفتهای بیشتری در تکنیک کریسپر خواهیم بود.
کوین اسوالت میگوید:
فقط یک پیشبینی قطعی میتوانم انجام دهم و آن این است که تکنیک کریسپر در سال ۲۰۱۸، میتواند موجب سرعت بخشی تحقیقات و امکانپذیر کردن درمان بیماریهای سخت شود. بیماریهایی که قبلا حتی تصور درمان آنها را نمیتوانستیم کنیم.
هانک گرلی، متخصص زیستی از دانشگاه استانفورد است که میگوید، پیشرفتهای مربوط به کریسپر حتی باید پا را فراتر از زمینه زیست پزشکی بگذارد.
او میگوید:
تیمهای تحقیقاتی مختلفی از تکنیک جدید و فوق العادهی کریسپر استفاده میکنند، این امکان وجود دارد که از این تکنیک در محیط های واقعی (غیرآزمایشگاهی) و البته به صورت کنترل شده بهره برد. میتوانم تصور کنم که در آیندهای نزدیک، جایزه نوبل پزشکی به کسانی که تکنیک ویرایش ژنی کریسپر را اختراع کردهاند، برسد.

البته باید بگوییم که محققان هنوز در آغاز راه اصلاح ژنی کریسپر هستند و چالشهای فنی زیادی پیش روی این تکنیک ژنتیکی نوظهور وجود دارد.
موضوعی که از بسیاری جهات در جامعه علمی بحثبرانگیز بوده، امکان ویرایش ژنی انسانهاست. اما هنوز چنین امکانی به وجود نیامده، اما چندین آزمایش امیدوارکننده در این زمینه انجام شده است
گرلی میگوید، با وجودی که آزمایشهای کلنیکی تکنیک کریسپر امسال آغاز میشود، اما برای نتیجهگیری از آنها باید منتظر بمانیم. در این مورد، توصیه او، کاهش سرعت پیشرفت و احتیاط بیشتر است. بحثی که جورج چرچ هم به آن اذعان دارد. به نظر پرفسور چرچ، امنیت، اولویت نخست چنین تحقیقاتی است و از این جهت حتی کاستن از سرعت مطالعات برای ایمن کردن تکنیک ویرایش ژنی کریسپر حتی از پیشرفتهای سریع هم مهمتر است.

باید منتظر آیندهای باشیم که تکنیک پیشرفته کریسپر رغم میزند. شاید سال ۲۰۱۸، سالی باشد که دانشمندان بتوانند حقیقتا به پتانسیل واقعی کریسپر دست پیدا کنند.
بهمن عبدی
- 11
- 4