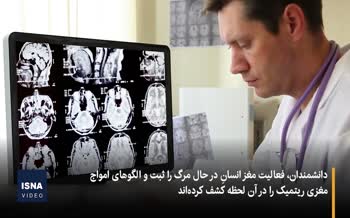
محققان مؤسسهی مغز و اعصاب بارو، آزمایشهایی در مورد بیماری اسکلروز جانبی آمیوتروفیک (ALS) یا بیماری لو گریگ انجام دادهاند که رابطهی پنج ژن جدید را با این بیماری تأیید میکند. نتایج این تحقیق که به پنج روش مختلف انجام شده است، در ژورنال Acta Neuropathologica منتشر شد و یافتههای قبلی در این پروژه مورد تأیید قرار گرفت. دکتر رابرت بوسر و همکارانش از فناوریهای ارئهشده توسط آیبیام واتسون شامل داروپژوهی واتسون (پلتفرم پژوهشی که ۲۸ میلیون مقالهی مدلاین و سایر منابع را در اختیار دارد) استفاده کردند.
این راه حل، پردازش زبان طبیعی پیشرفته، یادگیری ماشینی و تحلیلهای پیشگویانه را برای شناسایی روابط جدید بین ژنها، پروتئینها، داروها و بیماریها، مورد استفاده قرار میدهد. بهگفتهی دکتر بوسر، گسترش و تأیید یافتههای آنها بسیار هیجانانگیز است؛ زیرا زمان در این نوع پژوهشها بسیار اهمیت دارد. آنها بهطور جداگانه و به مدت طولانی، ۱۵۰۰ ژن و پروتئین را بررسی کردند. محققان با استفاده از این فناوری در آینده میتوانند درمانهای جدید و مؤثرتری برای بیماری ALS شناسایی کنند.
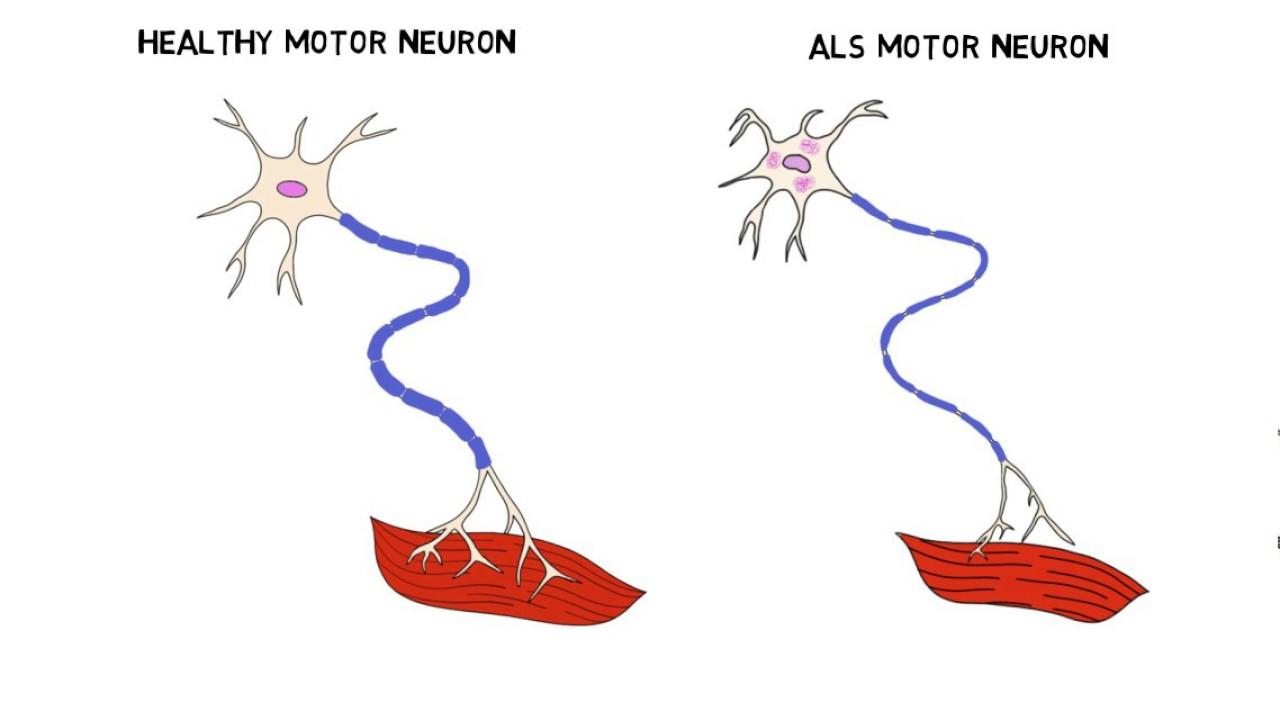
در بیماری نادر ALS با تخریب سلولهای عصبی، بیمار قدرت و توانایی حرکت و کنترل عضلات خود را از دست میهد و بهتدریج همهی عضلات تحلیل میروند. به مرور زمان فرد مبتلا، تواناییهای حرکتی خود را از دست میدهد؛ البته توانایی تفکر و حافظه این افراد معمولا تحت تأثیر این بیماری قرار نمیگیرد. معمولا مبتلایان به این بیماری مدت زیادی زنده نمیمانند.
بیماران مبتلا به این بیماری معمولا دچار ناتوانی حرکتی میشوند و ۳ تا ۵ سال پس از ابتلا به این بیماری جان خود را از دست میدهند. هرچند ۲۰ درصد این بیماران تا ۵ سال و ۱۰ درصد آنها تا ۱۰ سال زنده خواهند ماند. البته این مدت برای استیون هاوکینگ بین ۲ تا ۳ سال پیشبینی شده بود؛ اما او با همهی مشکلات و ناراحتیها همچنان به زندگی خود ادامه میدهد و برای مرگ لحظهشماری نمیکند. ایجاد رشتههای RNA مصنوعی نیز میتواند نقش مؤثری در توقف تولید پروتئینهای سمی داشته باشد. این نوع RNA خود را به RNA پیک که انتقال اطلاعات ژنتیکی را بهعهده دارد متصل میکند و از ساخت پروتئینهایی که به سلولهای عصبی آسیب میرساند، جلوگیری میکند.

این تحقیق بسیار مهم است؛ زیرا نشان میدهد الگوریتمهای هوش مصنوعی میتوانند باعث سرعت بخشیدن به تحقیقات آزمایشگاهی شوند. همچنین شواهد بیشتری در رابطه با نقش متابولیسم RNA در ALS ارائه میدهد.یافتهها نشان میدهند که بیش از ۳۰ ژن در ارتباط با بیماری ALS هستند و جهش در ۱۱ ژن که پروتئینهای متصلشوندهی RNA را کدگذاری میکنند، باعث ایجاد فرمهای خانوادگی ALS میشوند.
این پروتئینها در مورد اینکه چگونه ژنهای کدشده درون DNA هر سلول به پروتئینهایی تبدیل میشوند که تمام وظایف داخل سلول را انجام میدهند، نقش حیاتی دارند. تغییرات در این پروتئینها میتواند منجر به تغییر متابولیسم RNA و تولید پروتئین سمی در نورونهای حرکتی شود که به اختلال حرکتی و در نهایت فلج و مرگ کمک میکند.
DNA هر فرد برای بیش از ۱۵۰۰ پروتئین متصلشوندهی RNA رمزگذاری میکند و هنوز مشخص نیست که آیا دیگر پروتئینهای متصلشونده به RNA در بیماری ALS دخیل هستند یا نه؟ هزینه و زمان مورد نیاز برای بررسی تمام پروتئینهایی متصلشونده به RNA که در ژنوم ما رمزنگاری شدهاند، بسیار بالا است. آزمایشگاه باراو روی این موضوع که آیا داروپژوهی IBM واتسون میتواند به شناسایی پروتئینهای متصلشوندهی RNA مرتبط با ALS سرعت ببخشد یا خیر، مطالعه میکند.
دکتر بوسر و تیم او لیستی از ۱۱ پروتئین متصلشوندهی RNA با جهشهای شناختهشدهای که ALS را ایجاد میکنند، ارائه کردند. داروپژوهی واتسون، برای رتبهبندی دیگر ۱۵۰۰ ژن متصلشوندهی RNA که توسط ژنوم ما کدگذاری شدهاند و بهمنظور تعیین پروتئینهای جدید متصلشوندهی RNA مرتبط با ALS، از فهرستی از پروتئینها و مقالات ارجاعی به نشریات پزشکی، استفاده کرد.
تیم باراو، ۱۰ پروتئین متصلشوندهی RNA را بهوسیلهی پنج روش مختلف که شامل استفاده از نمونههای بافت و سلولهای بنیادی بیمار - که به نورونهای حرکتی متمایز شده است - تأیید کرد. آنها همچنین مجموعهای کوچکتر از پروتئینهای متصلشوندهی RNA را در پایین لیست بررسی کردند تا نشان بدهند تغییراتی که در ۱۰ پروتئین اول شناسایی شد، برای پروتئینهایی که در پایین لیست قرار دارند، مشاهده نشده است.
این کار میتواند توانایی داروپژوهی واتسون را در شناسایی صحیح این پروتئینها نشان دهد. نتیجه بسیار شگفتانگیز بود و پژوهشی که برای محققان میتوانست سالها زمان ببرد در عرض چند ماه انجام شد. هشت پروتئین از ۱۰ پروتئین مشخصشده توسط تیم باراو، تأیید شدند و نشان دادند که در ALS تغییر یافته است. پنج مورد از این ژنها در ALS مورد بررسی قرار نگرفتند که نشان میدهد هوش مصنوعی IBM میتواند ژنهای جدید و پروتئینهای مرتبط با این بیماری را پیشبینی کند.
پروتئینهای متصلشوندهی RNA در پایین لیست در ارتباط با ALS، تغییری نکردند. بیماری ALS درمان خاصی بهجز درمان علائم ندارد ولی بهتازگی استفاده از سلولهای بنیادی پیشنهاد شده است. دانشمندان اکنون در تلاش هستند با انجام آزمایشهای بالینی تأثیر این روشهای درمانی در بیماران مبتلا به ALS را مورد بررسی قرار دهند.
آنها امیدوارند با استفاده از نتایج این تحقیقات بتوانند به روشی برای درمان دیگر بیماریهای دستگاه عصبی مانند پارکینسون و آلزایمر دست یابند. برخی از پروتئینها مانند عوامل رشد بهآسانی جذب بافت عصبی میشوند و به نظر میرسد میتوانند از اعصاب حرکتی بدن نیز محافظت کنند. از آنجا که نمیتوان مولکولهای بزرگ را بهآسانی از طریق جریان خونی به دستگاه عصبی بدن منتقل کرد، برای استفاده از این مولکولها در فرآیندهای درمانی، باید آنها را بهطور مستقیم به عضلات تزریق کرد.
برخی از مولکولهای کوچک نیز نقش مهمی در تحریک دستگاه عصبی بدن دارند که میتوان آنها را بهراحتی به رگهای خونی منتهی به مغز منتقل کرد. استفاده از سلولهای بنیادی، روش دیگری است که مانع از پیشرفت بیماری خواهد شد. سلولهای بنیادی همانند پمپهای زیستی عمل میکنند و عوامل حیاتی مؤثر در رشد را به سلولهای عصبی آسیبدیده انتقال میدهند.
آزمایشهای انجامشده در افراد مبتلا به این بیماری نشان میدهند که سلولهای بنیادی میتوانند بهطور دقیق خود را به محل سلولهای عصبی آسیبدیده انتقال دهند. با پیشرفت تحقیقات زیستشناسی سلولی، دانشمندان امیدوارند روند کشف درمانهای جدید برای ALS را سریعتر کنند.
جمشید اللهویردی پور
- 17
- 2